近日,我校药学院孙敏捷教授与东南大学附属中大医院居胜红教授合作,在国际知名期刊Advanced Science(IF:17.521)发表最新研究成果:A Bio-Liposome Activating Natural Killer Cell by Illuminating Tumor Homogenization Antigen Properties。孙敏捷教授和居胜红教授为本文的通讯作者,中国药科大学为本文第一通讯单位。
近年来,肿瘤免疫疗法快速发展,展现出极佳的治疗效果,具有巨大临床应用前景。自然杀伤(NK)细胞是人体免疫系统的重要组成部分,能够发挥抗体依赖性细胞毒性(ADCC)作用以直接消除肿瘤细胞,对于抗肿瘤免疫至关重要。NK细胞还分泌细胞因子和趋化因子,募集树突状细胞(DC)聚集到实体瘤,从而增强CD8+ T细胞的抗肿瘤免疫作用。NK细胞的独特功能使得NK细胞疗法迅速发展,已成为免疫疗法的重要方向之一。然而,肿瘤细胞上抗原表达水平不同导致肿瘤异质性产生,限制了NK治疗的应用发展。因此,迫切需要增强肿瘤同质性来开发稳定、可控的NK细胞疗法。
针对上述问题,本论文采用“点亮肿瘤抗原属性”(ITHAP)策略,构建生物脂质体(Pt@PL-IgG)实现肿瘤细胞的重编程,以此促进NK细胞的募集并提高NK细胞对肿瘤细胞的识别能力。在这项研究中,通过血小板膜的自主驱动,Pt@PL-IgG成功靶向肿瘤细胞,并利用膜融合特性实现NK细胞可激活靶抗原IgG在肿瘤细胞上的植入,从而显著增强肿瘤细胞的免疫可识别性。体外研究表明,生物脂质体Pt@PL-IgG能显著活化41%的NK细胞,促使NK细胞发挥ADCC效应,杀伤约47%的肿瘤细胞,并有效促进44.5%的DC细胞成熟。另外在乳腺癌、胰腺癌、Burkitt's淋巴瘤、转移性黑色瘤等动物模型中,此生物脂质体均展现出了显著的抗肿瘤作用。ITHAP策略为医药、生物及仿生递送系统领域的免疫疗法拓展新的思路与方法。
该研究得到国家自然科学基金(81872817、92059202、82102202)和江苏省自然科学基金(BK20220831)的资助。
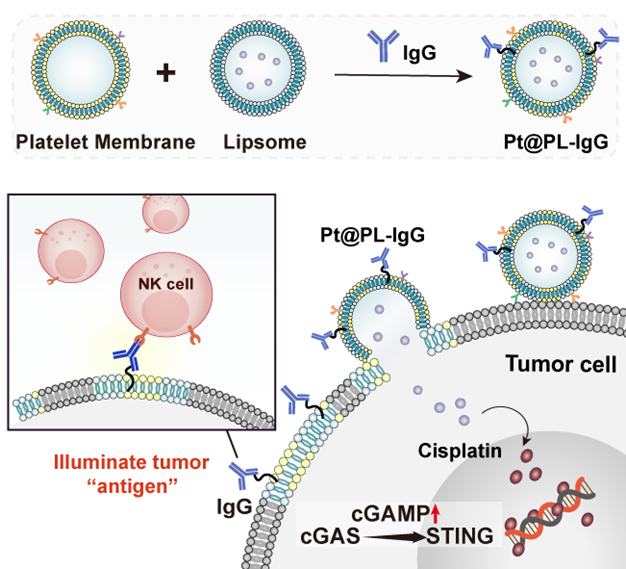
示意图 “点亮肿瘤抗原属性”(ITHAP)策略的构建
文章链接:https://onlinelibrary.wiley.com/doi/10.1002/advs.202205449?af=R
(供稿单位:药学院,撰写人:刘华,审稿人:黄欣、周天健)

